Европейската агенция по лекарствата одобри поставянето на трета игла
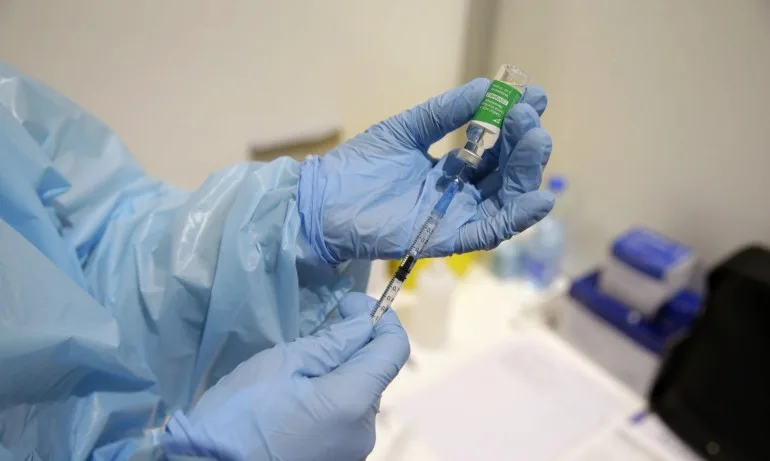
Лицата над 18 години с нормален имунитет могат да сложат дозата 6 месеца след втората
Бустерни дози от ваксините срещу Covid-19, разработени и произведени от BioNTech/Pfizer и Moderna, могат да бъдат предоставени на хора със силно отслабена имунна система, най-малко 28 дни след поставената им втора доза, реши Европейската агенция по лекарствата.
Препоръката е направена, след проучвания, които показват, че тя увеличава способността да се произвеждат антитела при пациенти с трансплантирани органи с отслабена имунна система.
„Въпреки че няма преки доказателства, че способността за производство на антитела при тези пациенти е създала защита срещу Covid-19, се очаква допълнителната доза да увеличи защитата поне при някои от тях“, се посочва в изявлението на ЕМА.
Агенцията подчерта, че европейците на възраст 18 и повече години с нормална имунна система би трябвало да получат бустерна (трета) доза най-малко 6 месеца след втората доза.
Важно е да се прави разлика между допълнителната доза за хора с отслабена имунна система и бустерните дози за хора с нормална имунна система, посочват от европейската лекарствена агенция.
Последната информация е за ваксината на Pfier/BioNTech, за която има данни, че повишава нивата на антитела, когато се дава бустерна доза приблизително 6 месеца след втората доза при хора на възраст от 18 до 55 години.
Въз основа на тези Комитетът заключава, че може да се обмисли поставяне на трета доза при хора с нормална имунна система най-малко 6 месеца след втората доза за лица на възраст 18 и повече години.
На национално ниво органите на общественото здравеопазване могат да издават официални препоръки за използването на бустерни дози, като се вземат предвид нововъзникващите данни за ефективността и ограничените данни за безопасност. Не е известно да има риск от възпалителни сърдечни заболявания или други много редки странични ефекти след бустерна доза, като EMA ще продължи да следи внимателно постъпващите данни.
В момента Комитетът оценява данните в подкрепа на бустерна доза за Spikevax (Covid ваксината на Moderna). ЕМА ще съобщи резултата, когато оценката приключи.
FaceBook Twitter Pinterest https://tribune.bg/bg/svqt/evropeyskata-agentsiya-po-lekarstvata-odobri-postavyaneto-na-treta-igla/








